Современные представления о грибковой патологии пищеварительного тракта
В гастроэнтерологии, как и в других областях медицины, динамично развиваются методы диагностики и лечения грибковых инфекций на основе изучения физиологии, микробиологии, фармакологии, молекулярной патологии и медицинской генетики. Детально изучаются уже
В гастроэнтерологии, как и в других областях медицины, динамично развиваются методы диагностики и лечения грибковых инфекций на основе изучения физиологии, микробиологии, фармакологии, молекулярной патологии и медицинской генетики. Детально изучаются уже известные варианты болезни и описываются редкие и новые нозологические формы.
Грибы, являясь нормальными комменсалами желудочно-кишечного тракта (ЖКТ), становятся патогенными при определенных условиях. Это касается в основном дрожжеподобных грибов Candida spp., виды и даже штаммы которых различаются по факторам агрессии, способности к адгезии и инвазии [15].
Candida albicans — наиболее частый возбудитель кандидоза ЖКТ. Однако в последние годы большую роль играют Candida non-albicans (C. krusei, C. tropicalis, C. kefyr, C. glabrata, C. parapsilosis); у лиц с иммунодефицитом их пропорция составляет более 50%, при «относительно нормальном» иммунитете — 15%.
Грибы Candida (условно-патогенные микроорганизмы) заселяют ЖКТ — этот феномен называется колонизацией, — процесс протекает бессимптомно. Исследование взрослых здоровых добровольцев показало, что Candida albicans присутствует в орофарингеальной зоне у 20–30% из них, в тонком кишечнике — у 50–54%, в толстом кишечнике — у 55–70% и в фекалиях — у 65–70% [9, 13]. При исследовании состава микрофлоры полости рта у населения нескольких стран Европы обнаружено присутствие грибов у 10–25% людей, в кале — у 65–80% [11, 17]. Детально изучена колонизация зева грибами Candida у больных гемобластозами: она составила 33% [8]. В биоптатах гастродуоденальных язв в 17–30% случаев находят дрожжеподобные грибы [12]. У 50% жителей Германии в микробиоте кишечника присутствуют грибы, а у онкогематологических больных колонизация кишечника составляет 63–65% [10, 11]. Нельзя забывать, что у 0,8–4% пациентов грибы случайно обнаруживаются в пузырной и протоковой желчи, а при желчнокаменной болезни — у 15–20%.
Бессимптомное пребывание грибов в ЖКТ может прекратиться, когда они приобретают патогенные свойства. Так, у больных с нейтропенией грибы из кишечника могут диссеминировать в печень, селезенку и легкие, а в катетер-ассоциированной ситуации грибы попадают непосредственно в ток крови, достигают сердца и почек.
Дрожжеподобный гриб Cryptococcus neoformans в патологии ЖКТ как этиологический фактор играет незначительную роль. Он чаще поражает нервную систему и, диссеминируя из первичного очага, вовлекает гастроинтестинальный тракт. Описаны единичные случаи (чаще посмертно) криптококкового эзофагита, стоматита, терминального илеита, колита, холецистита, панкреатита. Как правило, они относились к ВИЧ-серопозитивным больным, а также к пациентам, страдающим гипергаммаглобулинемией Е с рецидивирующими абсцессами печени и перианальной зоны.
Болезни ЖКТ, вызванные диморфными патогенными грибами (II группы патогенности), зарегистрированы в Южной Америке, но время от времени встречаются как спорадические случаи по всему миру. Большинство диморфных грибов в природе существуют в мицелиальной форме, попав в организм они трансформируются в дрожжеподобные и приобретают патогенные свойства. Пероральный путь проникновения не характерен, в ЖКТ эти грибы попадают при диссеминации из других органов. Blastomyces dermatitidis продуцирует гранулематозное повреждение в желудке и тонком кишечнике. Coccidioides immitis, Histoplasma capsulatum, Paracoccidioides brasiliensis и Sporothrix schenckii поражают кишечник только при диссеминации из кожных очагов и респираторного тракта [6, 15].
Грибы Aspergillus spp. редко вызывают болезнь ЖКТ, только в случаях стойкой нейтропении, кахексии и при других отягощающих состояниях.
Грибы класса Zygomycetes могут привести к развитию интестинального зигомикоза, который, как правило, ассоциирован с амебиазом, голоданием, диабетическим кетоацидозом, почечным гемодиализом. Penicillium spp. и Geotrichum поражают ЖКТ также редко.
Дрожжеподобные, плесневые и некоторые диморфные грибы — это условно-патогенные, оппортунистические микроорганизмы, которые широко распространены в окружающей среде и легко могут попадать на кожу, слизистые оболочки полости рта, гениталий и в дыхательные пути. Кроме того, для грибов характерен эндогенный способ существования (миконосительство).
ЖКТ покрыт слизистой оболочкой, состоящей из двух компонентов — поверхностного скользкого, слизистого слоя, по которому микроорганизмы легко продвигаются вдоль всего ЖКТ, и более глубокого плотного гликопротеинового слоя с остатками сиаловой кислоты, который формирует физиологический барьер. Адгезия и последующая инвазия грибов через этот плотный слой возможны только благодаря продукции грибами протеолитических «ферментов инвазии»: коагулазы, каталазы, козеиназы, фосфолипазы, а также фибриллярных протеиновых комплексов и эндотоксинов [15].
При физиологическом благополучии между макро- и микроорганизмами существует определенное равновесие, в котором играют роль, с одной стороны, факторы устойчивости организма к микроскопическим грибам, а с другой — факторы патогенности грибов.
Устойчивость организма зависит от принадлежности к группам риска и состояния иммунной системы.
Перечислим факторы риска развития грибковых инфекций ЖКТ.
- Поражение слизистых оболочек полости рта (красный плоский лишай, зубные протезы, травмы, ксеростомия, использование гормональных ингаляторов).
- Хронические заболевания ЖКТ (атрофический гастрит, гипоацидность желудка, ахалазия, бульбит, эрозивно-язвенные заболевания пищевода и кишечника, дивертикулез, полипоз, гастроэзофагальная рефлюксная болезнь, энтероколит, болезнь Крона, синдром раздраженной кишки, обсемененность желудка Helicobacter pylori, дисбиоз, микст-инфекция кишки).
- Травмирование слизистой оболочки (ожоги, пищеводно-желудочный зонд, эндотрахеальная интубация).
- Беременность.
- Период новорожденности (недоношенность, массивность инфекции при прохождении через родовые пути, естественное несовершенство иммунной системы).
- Пожилой возраст (старение иммунной системы, сопутствующие заболевания, уменьшение амплитуды продольных сокращений пищевода, силы сокращений сфинктеров, нарушение процессов всасывания и т. д.).
- Онкологические и гематологические заболевания (нейтропения).
- Эндокринопатии (особенно сахарный диабет).
- СПИД, ВИЧ-инфицированность.
- Трансплантационные операции.
- Состояния, требующие пребывания в отделениях интенсивной терапии.
- Тяжелые аллергические заболевания.
- Прием антибиотиков, цитостатиков, гормонов и других химиопрепаратов в неадекватных дозах.
- Нарушения питания, в том числе голодание с целью снижения веса.
- Алкоголизм, курение, наркомания.
Важным компонентом защиты от инвазии ЖКТ является иммунная система, ассоциированная с кишечником. Клеточная часть этой системы включает в себя интраэпителиальные лимфоциты, которые препятствуют дисперсии возбудителя через lamina propria и агрегации в пейеровых бляшках. В-лимфоциты кишечника участвуют в продукции секреторных IgA и IgM, которые уменьшают способность грибов к адгезии.
Т-клетки здорового организма продуцируют защитный интерферон, усиливают фагоцитоз, активируют Т-цитотоксические лимфоциты. СД4 и СД8 укрепляют местный иммунитет в ЖКТ. Причем оказалось, что цитотоксичность СД8 играет более существенную роль в предотвращении заболевания, чем предполагали раньше.
В защите важны также макрофагальный и нейтрофильный фагоцитоз, препятствующие диссеминации грибковой, особенно кандидозной инфекции.
У ВИЧ-пациентов и больных с нейтропенией, у которых фагоцитоз резко подавлен, местная инвазия и диссеминация инфекции наступают очень быстро. Известно, что нейтрофилы хотя и не могут полностью защитить слизистую оболочку ЖКТ от «атаки» грибов, но благодаря собственной «киллерной» субстанции через специфический механизм запускают активацию комплемента, который усиливает фагоцитоз. Следует отметить, что фагоцитоз особенно важен при кандидозной инфекции, но «не работает» в тканях против капсулированных криптококков и большинства мицелиальных грибов.
Нормальные биохимические, гистохимические и физиологические процессы в ЖКТ, своевременная регенерация эпителиоцитов, кислотно-ферментативный барьер, полноценная перистальтическая активность также являются защитными факторами, которые препятствуют проникновению грибковой и бактериальной флоры [4]. Роль желудочной кислоты в предотвращении внедрения грибов в слизистую неоспорима. В среде с пониженной кислотностью грибы Candida приобретают патогенные свойства, появляются вегетирующие формы, образуется псевдомицелий или мицелий, повреждающий слизистую оболочку. У ВИЧ-инфицированных лиц, для которых характерна ахлоргидрия, попадающие с пищей грибы Candida могут вызывать кандидоз желудка, в то время как у людей с нормальным иммунитетом эта локализация встречается редко. Роль кислотности желудочного сока в развитии бактериальной и грибковой инфекции кишечника не подтверждена.
Облигатные микроорганизмы желудка и кишечника (аэробные лактобациллы, анаэробные бифидум-бактерии, нормальная кишечная палочка и др.) также играют защитную роль. Применение антибиотиков убивает, наряду с патогенными, и эти «полезные» бактерии, открывая на слизистой оболочке рецепторы адгезии для грибов [2].
Нельзя не упомянуть также о Helicobacter pylori, который довольно часто обитает в желудке, вызывает гастрит, язвенную болезнь, а иногда оказывает канцерогенное воздействие. В свою очередь, лечение хеликобактериоза антибиотиками приводит к активации грибов Candida и кандидозу желудка [1]. Ассоциации грибов с Helicobacter pylori и другими бактериями в ЖКТ встречаются нередко, что требует продуманного адекватного подхода к тактике лечения.
В желудке могут также присутствовать Saccharomyces cerevisiae и некоторые виды Candida, способные сбраживать и ферментировать до винного спирта сахара, попадающие с пищей в желудок. Этот феномен называется синдромом «пивоваренного завода» [14].
Вирулентность грибов, патогенные факторы, как и полисахариды (маннаны), плазмокоагулаза, эндотоксины, липиды, глюкоконъюгаты, влияют на развитие заболевания. Даже от внутривидовых способностей грибов зависит, разовьются ли в каждом конкретном случае кандиданосительство или болезнь [13]. Например, серотип В Candida albicans считается более вирулентным и наиболее распространенным возбудителем орофарингеального кандидоза у ВИЧ-инфицированных больных, также он поражает генитоуринарную систему и нередко выделяется из зева у гомосексуалистов.
Микроскопически факторы агрессии грибов Candida проявляются формированием ростковых трубок, псевдогифов и истинного мицелия — за счет них грибы могут врастать в стенку фагоцитов. Однако дрожжи, которые не способны продуцировать мицелий, такие, как Candida glabrata, Cryptococcus neoformans, также могут вызывать заболевания ЖКТ.
Причины аспергиллеза
Возбудителями человеческого аспергиллеза могут являться такие разновидности плесневых грибов Aspergillus, как A. Fumigatus, A. Flavus, A. Terreus, A. Niger, A. Clavatus и A. Nidulans. Аспергиллы – это гетеротрофные и аэробные грибы, способные расти при температуре не более 50°С, а также сохраняться при замораживании или высушивании в течение длительного срока.
В окружающей среде данные грибы максимально распространены, кроме прочего, благоприятные условия для роста и размножения аспергилл имеются в кондиционерах, душевых и вентиляционных системах, старых пыльных книгах и вещах, в комнатах с сырым потолком и стенами, хранящихся долгое время пищевых продуктах, различных растениях и так далее.
Заражение данным недугом в большинстве случаев происходит ингаляционным путем, который заключается во вдыхании пылевых частиц, содержащих мицелий плесневого гриба.

В других случаях появление грибковой инфекции является возможным при инфицировании в ходе проведения инвазивных медицинских процедур, например, эндоскопической биопсии, бронхоскопии, пункции околоносовых пазух и прочих сложных врачебных вмешательств. Не исключается контактный путь получения и передачи заболевания через пораженные слизистые оболочки и кожные покровы. Кроме этого, возможно получение алиментарного инфицирования после употребления в пищу продуктов питания, содержащих аспергиллы, например, мяса.
Помимо экзогенного развития инфекции, медицине известны случаи трансплацентарного развития инфекции и аутозаражения данной болезнью при активации грибков, которые обитают на кожных покровах, слизистой оболочке зева и в дыхательных путях человека.
К факторам риска развития болезни относятся хронические заболевания дыхательной системы, иммунодефициты любого происхождения, дисбактериоз, сахарный диабет, травмы ожогового характера, прием кортикостероидов, цитостатических и антибиотических препаратов, а также факт проведения лучевой терапии. Распространены случаи развития микоза смешанной этиологии, который вызывается различными видами грибков – кандидой, аспергиллами и актиномицетами.

Aspergillus под микроскопом
Как защититься от заражения плесневыми грибками?
- Нужно соблюдать осторожность при разборке старых, ветхих дач, при использовании лежалого строительного материала. Грибки, поселившиеся на дереве, особенно опасны.
- Хотя грибы на пищевых продуктах менее агрессивны, тем не менее, небольшое пятно плесени на хлебе нужно тщательно вырезать, а если плесень появилась в нескольких местах, хлеб лучше в пищу не употреблять.
- Загнивающие места на яблоке можно удалить, а вот заплесневевшие сочные фрукты и овощи – помидоры, груши, персики, абрикосы, особенно если плесень появилась вокруг косточки, — придется выбросить.
- Без колебания выливайте компоты, соки и сиропы с пятнами плесени, а вот в конфитюрах, варенье с высоким содержанием сахара достаточно удалить верхний толстый слой.
- Нельзя есть заплесневевшие ядра орехов с горьким затхлым привкусом. Следует отказаться от творога и других заплесневелых молочных продуктов.
- Небольшие пятна плесени на сыре можно удалить, а если плесень образовалась внутри головки, рисковать не стоит. Правда, есть сыры, например, рокфор, которому плесень придает особый пикантный привкус, но если у вас грибковая инфекция, от такого любимого многими гурманами лакомства придется на время отказаться.
Заниматься самолечением в этой ситуации опасно. Распознать грибковое заболевание в самом начале болезни можно лишь при своевременном обращении к специалистам, занимающихся лечением пораженных органов или систем (гинекологам, гастроэнтерологам и т.д.) или микологам – специалистам по грибковым инфекциям. Микологические исследования позволяют уточнить природу заболевания, отличить грибковое заболевание от бактериального.
Врач подберет специальные противогрибковые препараты нового поколения, назначит общеукрепляющие процедуры и мультивитаминные комплексы. Нередко назначаются ферменты, улучшающие функции пищеварительной системы, регуляторы кишечной микрофлоры, желчегонные средства и лекарства, защищающие печень.

Фото: fahroni / freepik.com
Одновременно с противогрибковым лечением большое внимание уделяется специальной «антигрибковой» диете. Эта диета предусматривает отказ от продуктов, богатых углеводами, поскольку нарушение углеводного обмена приводит к повышению уровня сахара в крови, а сахар — отличная среда для грибов. Не рекомендуются макаронные изделия, блюда из круп, а также все, что приготовлено с использованием дрожжей: пиво, квас, шампанское, сдобные булочки, пирожные, торты. Даже хлеб можно есть только сегодняшний, поскольку на второй-третий день в нем может начать расти плесень.
Чтобы на время приема сильнодействующих препаратов разгрузить печень, врачи рекомендуют воздержаться от жирного мяса (свинины, баранины, копченостей, наваристых бульонов, жареных блюд, а также от мяса утки и гуся). Можно оставить в рационе телятину, говядину, курицу, рыбу в отваренном или тушеном виде. Рекомендуется употреблять овощи, нежирный творог и сметану, а также кисломолочные продукты – кефир и ацидофилин.
Патогенез отомикоза
Ушная раковина представляет собой эластический хрящ, покрытый кожей. Полость ушной раковины воронкообразно углубляется и переходит в наружный слуховой проход. Функцией данной структуры является улавливание звуков, их концентрация и направление в наружный слуховой проход.
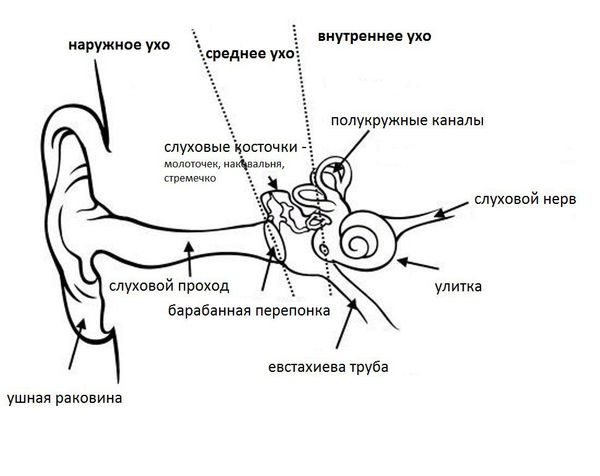
Наружный слуховой проход представляет собой полую трубку диаметром 0,3-1,0 см и длиной около 2,5 см у взрослых. Он состоит из хрящевой части, которая является продолжением хряща ушной раковины, и костной части, занимающей 2/3 наружного слухового прохода. Кожа в наружных отделах слухового прохода содержит волосы, сальные и серные железы [2] .
Барабанная перепонка проводит наружные колебания и является границей, которая отделяет наружное ухо от среднего. Среднее ухо состоит из центральной части, которая представлена барабанной полостью. Кпереди и книзу от барабанной полости находится слуховая труба (евстахиева труба). Кзади от барабанной полости находятся сосцевидные ячейки.
В норме полость среднего уха стерильна, т. е. грибков и других микробов в ней нет. Их попаданию препятствует изоляция от внешней среды за счёт барабанной перепонки, дренажной функции слуховой трубы и местного иммунитета. Тем не менее, грибы могут проникать в среднее ухо через слуховую трубу из глотки либо через систему крово- и лимфообращения.
Основными патогенетическими звеньями возникновения микоза являются адгезия грибов, т. е. прикрепление гриба к коже или раневой поверхности, колонизация гриба и инвазивный рост [7] . При тяжёлой форме микоза может произойти генерализация процесса, т. е. проникновение возбудителя в кровь с распространением по организму и появлением вторичных очагов грибковой инфекции в различных органах и тканях. Микозы могут выступать своеобразными «маркерами» нарушения иммунитета, так как иммунодефицит является одним из основных моментов в патогенезе грибковой инфекции.
Болезнь Лайма: заразна ли она?
После укуса клеща происходит проникновение возбудителя в кожу человека и дальнейшее его размножение в ней. Затем микроорганизмы распространяются в лимфоузлы, расположенные рядом с местом укуса. Спустя несколько суток боррелии попадают в кровоток и разносятся по всему организму, попадая сердце, нервную систему, суставы, мышцы. В иммунной системе начинается выработка антител против боррелий, однако даже при их высоких титрах полное уничтожение возбудителя не достигается.
Образовавшиеся вследствие болезни Лайма иммунные комплексы запускают аутоиммунный процесс (антитела начинают бороться с собственными тканями организма), что приводит к хроническому течению заболевания. При гибели возбудителя в организм выбрасываются токсические вещества, в результате чего состояние больного значительно ухудшается.
Больные, зараженные клещевым боррелиозом, не опасны для окружающих и не являются источником инфекции.
Симптомы аспергиллеза: Повышение температуры, затруднение дыхания, густая мокрота с коричневым оттенком, кашель.
1.Первым делом надо устранить аллерген.
2.Необходимо определить причину, возбудитель заболевания и устранять его. Это делает врач.
3.Укрепление иммунной системы жидкими пробиотиками Бифидум БАГ и Трилакт.
Бифидобактерии и лактобактерии – естественные безопасные иммуномодуляторы.
Бифидо- и лактобактерии нормализуют иммунитет на 2 уровнях:
1 уровень ВРОЖДЕННАЯ иммунная система
2 уровень АДАПТИВНАЯ (приобретенная) иммунная система
Пробиотики активизируют местную защиту, на слизистой полости рта, носоглотки, миндалин, в бронхах и в легких и далее в лимфоидных органах желудочно-кишечного тракта (общий иммунитет).
Рекомендуемая схема приема препарата в комплексной терапии аспергиллезов для детей от 12 лет и взрослых перорально (внутрь) +местно (на слизистую носа, для полоскания горла) для снятия отека, вытеснения грибов и иммуностимуляции всего организма
Длительность курса 40 дней
Время и дозировки приема препаратов
Утром –доза Трилакт с полосканием полости рта и горла с проглатыванием ½ флак
Днем – доза Экофлор 2 пак Вечером -доза Бифидум БАГ полоскание полости рта и горла с проглатыванием 1/2 флак
Капли в нос 3 раза в день в положении с сильно запрокинутой головой по 3-4 капли Трилакт в каждый носовой ход. На 1 часть Трилакт 2 части физ. раствора (10 дней)
Утром –доза Трилакт с полосканием полости рта и горла и проглатыванием ½ флак
Вечером – доза Бифидум ½ флак
Капли в нос 3 раза в день в положении с сильно запрокинутой головой по 3-4 капли Бифидум БАГ в каждый носовой ход. На 1 часть Бифидум 2 части физ. раствора (10 дней)
Утром –доза Трилакт ½ флак Вечером–доза Бифидум ½ флак
Полоскание горла : полоскать горло 5 мл Трилакт или Бифидум БАГ 4-5 раз в сутки в разведении с физ. раствором от1:1 к 1:2. После полоскания препараты проглатывать.
Закапывание в нос: вводить Трилакт или Бифидум БАГ по 3-4 капли в каждый носовой ход 2-3 раза в день в положении с сильно запрокинутой головой в разведении от 1:1 до 1:5 с физ. раствором ( для уменьшения отека слизистой оболочки носоглотки).
